氨基钠是一个无机化合物,化学式为NaNH2。室温下纯品为白色固体,试剂常带金属铁而呈灰色。氨基钠与水强烈反应,是有机合成中常用的强碱。
氨基钠可由钠与氨气反应, 或硝酸铁催化下钠与液氨的反应来制备。后者反应在氨沸点(约-33°C)时反应最快,也更常用:
NaNH2为类盐固体,晶格中 钠原子为四面体结构。 溶于氨时,NaNH2溶液存在Na(NH3)6+和NH2−离子,可导电。
工业上,氨基钠是制取靛青染料、肼和氰化钠等工业品的原料。 可用于干燥液氨或氨气,其液氨溶液也是有机化学中常用的强碱。氨基钠碱性很强而且亲核性很弱,但不易溶于大多数溶剂中,因而已被氢化钠、双(三甲硅基)氨基钠(NaHMDS)以及二异丙基氨基锂(LDA)等类似试剂所取代。
氨基钠可使偕二溴代烷失去两分子溴化氢,生成炔烃。如下图制备苯乙炔的反应所示:
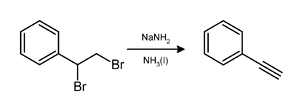
也可使分子脱去氯化氢和/或乙醇, 如下图中制备1-乙氧基-1-丁炔的反应:
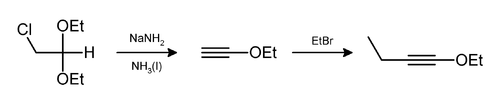
无β-氢可消除时,则可发生成环反应,见下面合成亚甲基环丙烷的反应:
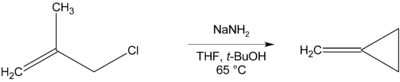
环丙烯、 吖丙啶和环丁烷 环系都可通过此法制取。
氢碳酸,包括末端炔烃、甲基酮、环己酮、苯乙酸及衍生物和二苯甲烷 等,都可被液氨中的氨基钠脱去质子。用两分子氨基钠时,乙酰丙酮失去两个质子生成双负离子:

吲哚 和哌啶 也可发生类似反应。
氨基钠会与水猛烈反应生成氢氧化钠和氨,且在空气中可燃烧生成钠氧化物及二氧化氮:
氨基钠应当储存在密闭容器中,最好以氮气保护。当放置于密闭性不好的容器中时,氧气和水不充足,有可能生成爆炸性的氧化产物从而使固体泛黄棕色。此类试剂应当尽快销毁,方法为向氨基钠的烃类溶剂悬浮液中小心加入乙醇。
氨基钠可能会对皮肤、眼部及黏膜有强腐蚀性,应当留心空气中悬浮的氨基钠粉末。
