溶剂效应是指溶剂所产生的一连串化学反应,会影响主要化学反应的反应速率、反应平衡、溶解度、稳定性甚至是反应机理;换而言之,化学反应中的热力学和动力学可借由选择适当溶剂来控制。
溶质在溶剂中溶解时会与溶剂产生相互作用,其过程称为“溶剂化(solvation)”,取决于双方(指溶质和溶剂)的自由能 (free energy)变化,而自由能在反应中受多个因素影响。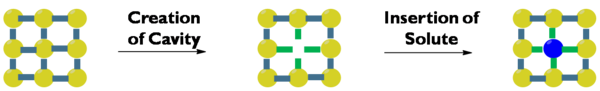
进行溶剂效应的静态模拟时,我们将焦点放在溶剂效应的两个主要作用上:一是短程作用,是指溶剂和溶质分子的反应中心所产生的相互作用(如:配位键、氢键的形成等);另一个是远程作用,极性溶剂、溶质分子两个偶极距间的静电相互作用。
在进行静态模拟可使用的三种溶解模型:
短程作用的模拟,大多采用QM法(QM methods),研究溶剂分子的活性中心,考虑键的生成对反应区域和反应过渡态结构和能量的影响。
远程作用需要考虑较多变因,故需要借助物理模型来做近似处理;连续介质(Continuum)模型有很多,其中常用的是极化连续介质模型(Polarized Continuum Model, PCM)。PCM最早于1981年由Tomasi教授(意大利比萨大学)提出 。
溶剂效应涉及到三个概念溶剂空腔形成(cavity formation)、分散排斥(dispersion-repulsion)和静电交互作用(electrostatic interaction)
以上三大概念所提到的能量增减总和即为溶剂化自由能(free energy of solvation)。
不同的溶剂可能会因为反应物及产物的稳定性差异而影响反应的平衡常数,反应会朝向产物较稳定的方向平衡。反应物或产物可利用任何与溶剂所产生的非共价相互作用(如氢键、偶极-偶极相互作用、凡得瓦力等作用)来提升稳定性。
酸或碱的电解平衡会受溶剂变化影响。但溶剂不仅仅是受其酸性或碱性影响,同时也受到其介电常数(dielectric constant)和其优先溶剂化(preferentially solvate)影响,而使特定反应的酸碱平衡较稳定;换而言之,即溶解能力及介电常数的变化皆可以影响的溶液的酸碱值。
在上表中可以看出水是极性最大的溶剂,第二为DMSO,最后为氰化甲烷。
再思考下面的酸离解公式:
水是上表中极性最大的溶剂,相较于二甲基亚砜或氰化甲烷,水使得离子化的物质能产生更高的稳定度;由此可知,水中的酸性会比二甲基亚砜或氰化甲烷来得低,如下表中可看出,pKa值在25℃时之值为氰化甲烷(ACN)>二甲基亚砜(DMSO)>水。
各种1,3 - 二羰基化合物(1,3-dicarbonyl compounds)可以透过互变异构物(tautomeric forms)的形式存在,如图所示。
1,3 - 二羰基化合物最常在环烯醇(cyclic enol)(为顺式异构体)和二酮(diketo)这两种结构间互相转换。
互变异构作用的平衡常数如下:
溶剂对乙酰丙酮(Acetylacetone)互变异构的平衡常数之影响如下:

